スチル病に伴うマクロファージ活性化症候群(MAS)を発症している患者、又は全身性エリテマトーデスに伴うMASを対象とする抗IFNγモノクローナル抗体エマパルマブの治験協力のお願い
2023年09月19
日
日本小児リウマチ学会
会員各位
スチル病に伴うマクロファージ活性化症候群(MAS)を発症している患者、
又は全身性エリテマトーデスに伴うMASを対象とする
抗IFNγモノクローナル抗体エマパルマブの治験協力のお願い
この度、当学会に開発企業のSobi社よりマクロファージ活性化症候群(MAS)へのエマパルマブ(抗 IFN-γ モノクローナル抗体)の治験促進への協力依頼がございました。治験対象は小児及び成人のスチル病(全身型若年性特発性関節炎(sJIA)及び成人スチル病(AOSD))でMASを合併している患者様、さらに小児及び成人の全身性エリテマトーデス(SLE)でMASを合併している患者様です。
MASはサイトカインストームを病態の主座とする危急的かつ予後不良な疾患であり、IFN-γはMASの病態において、中心的な役割を果たすサイトカインです。抗 IFN-γ モノクローナル抗体のエマパルマブは、血中の遊離IFN-γや IFN-γ 受容体に結合したIFN-γを阻害することにより、IFN-γを介したマクロファージの活性化やサイトカインの放出を抑制します。その結果、炎症の抑制、臓器障害の進展防止、寛解導入が期待されます。
現在、本邦においても新規適応取得に向けて第Ⅱ/III相試験が進行中です。しかしながら、本症は稀少疾患であり、症例登録が極めて芳しくない状況が続いています。この度、会員の先生方には、治験対象として該当する可能性があるMASと診断された、もしくはMASが疑われる患者様の治験施設への積極的なご紹介をお願いする次第です。
治験概要および主な参加基準の概略、治験実施中の医療機関を下記に記しましたのでご参照ください。患者様をご紹介頂く際は、先ずは各医療機関の治験責任医師にご連絡をお願いします。なお、本治験には下記以外にも選択基準・除外基準があり、ご紹介頂きました患者様が治験へ参加頂けない場合もございます。ご紹介の際は、患者様にその可能性も含めお伝え頂ければ幸いに存じます。エマパルマブの本邦における適応取得は、重要な臨床的課題です。恐縮ではございますが、本治験の推進にご協力の程よろしくお願い申し上げます。
またご不明の点がございましたら、下記に治験責任医師にご連絡をお願いいたします。
【治験概要】
■治験課題名
スチル病(全身型若年性特発性関節炎及び成人スチル病を含む)の小児及び成人患者で、マクロファージ活性化症候群(MAS)を発症している患者、又は全身性エリテマトーデスの小児及び成人患者でMASを発症している患者を対象に、エマパルマブの有効性、安全性及び忍容性、薬物動態及び薬力学を検討する、2コホート、非盲検、単独投与群、多施設共同試験(治験実施計画書番号:NI-0501-14)
■治験目的
以下のコホートの患者の治療における エマパルマブの有効性を確認する。
・コホート 1:sJIA 及び AOSD に伴う MAS
・コホート 2:小児及び成人 SLE に伴う MAS
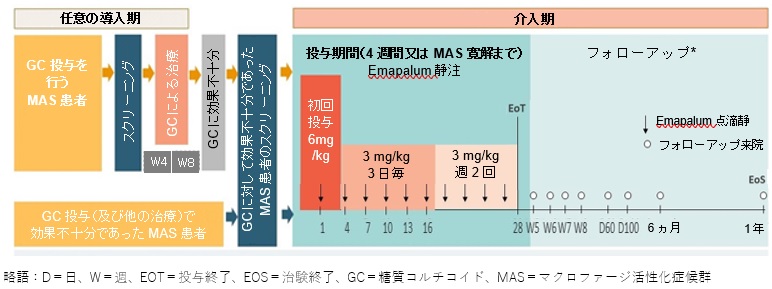
■試験デザイン
■sJIA患者の主な参加基準
●準治療に従った3日間以上の経静脈的高用量グルココルチコイドで効果不十分であること
※急激な悪化の場合、治験責任医師の判断により、3日未満で介入期に移行可能
●MASの診断は治療担当のリウマチ専門医が以下を確認して確定する。
発熱患者で、フェリチンが>684 ng/mL
かつ、以下のいずれか2つ:
血小板数:≦181×109/L
AST値:>48 U/L
トリグリセリド:>156 mg/dL
フィブリノゲン濃度:≦360 mg/dL
●sJIA 診断が確定している患者。sJIA 発症時に MAS が発現した患者については、sJIA が強く推定される場合、適格性を満たすものとする。
■目標症例数
・コホート 1:sJIA 及び AOSD に伴う MAS 25例
・コホート 2:小児及び成人 SLE に伴う MAS 16例
■登録期間
2023年12月末終了予定
【治験実施医療機関】()内 = 治験責任医師
聖マリアンナ医科大学病院(森 雅亮)
東京医科歯科大学病院 (清水正樹)
大阪医科薬科大学病院 (杉田侑子)
横浜市立大学附属病院 (伊藤秀一)
令和5年9月8日
小児リウマチ学会 薬事委員会
委員長 伊藤秀一